Spis treści
Co to są materiały hydrofilowe i hydrofobowe?
Materiały hydrofilowe to substancje, które wykazują doskonałą interakcję z wodą, zwiększając powierzchnię kontaktu z tym rozpuszczalnikiem. W ich skład wchodzą:
- polisacharydy,
- białka,
- niektóre polimery syntetyczne.
Z kolei materiały hydrofobowe, np. oleje i woski, mają właściwości odpychające cząsteczki wody, co skutkuje powstawaniem kropli na ich powierzchni. Hydrofobowość oznacza, że dana powierzchnia nie ma tendencji do przylegania do cieczy. To zjawisko ma istotne znaczenie w takich dziedzinach jak:
- budownictwo,
- przemysł tekstylny.
Chemiczne cząsteczki o długich łańcuchach węglowodorowych często przyjmują właściwości hydrofobowe, co dodatkowo sprzyja ich odpychaniu wody. Zrozumienie tych cech jest kluczowe, ponieważ materiały hydrofilowe i hydrofobowe znajdują swoje zastosowanie w wielu dziedzinach. Ich właściwości mogą znacząco wpłynąć na efektywność procesów technologicznych, takich jak filtracja czy produkcja emulsji.
Jakie są różnice między materiałami hydrofilowymi a hydrofobowymi?
Materiały hydrofilowe i hydrofobowe różnią się głównie swoją budową chemiczną oraz tym, jak wchodzą w interakcje z wodą. Hydrofilowe substancje, o charakterystyce polarnej, z łatwością rozpuszczają się w wodzie. Do najpopularniejszych przykładów należą:
- białka,
- polisacharydy,
- które efektywnie wchłaniają wodę.
Z kolei materiały hydrofobowe, które mają strukturę niepolarną, słabo łączą się z wodą, a ich powinowactwo do tego rozpuszczalnika jest niskie. W rezultacie woda na ich powierzchni nie zwilża ich, a tworzy charakterystyczne krople. Przykładem cząsteczek hydrofobowych są:
- oleje,
- woski,
- które zawierają długie łańcuchy węglowodorowe, co podnosi ich zdolność do samoczyszczenia.
Kąt zwilżania również odgrywa kluczową rolę w tych różnicach; materiały hydrofilowe charakteryzują się niskim kątem zwilżania, a ich hydrofobowe odpowiedniki – wysokim, co sprawia, że kontakt z wodą jest dla nich trudniejszy. Te właściwości mają istotne znaczenie w różnych dziedzinach, takich jak:
- budownictwo,
- przemysł tekstylny,
- produkcja emulsji.
Odpowiedni wybór materiałów może znacząco wpłynąć na efektywność procesów technologicznych. Wiedza na temat tych właściwości pozwala na skuteczniejsze optymalizowanie materiałów w wielu zastosowaniach.
Co to jest hydrofobowość i jakie ma znaczenie dla materiałów?
Hydrofobowość to fascynująca właściwość materiałów, która sprawia, że są one w stanie odpychać wodę. Dzięki temu krople wody nie wnikają w ich strukturę, a zamiast tego formują się na powierzchni. To naturalne zjawisko znajduje zastosowanie w wielu dziedzinach, gdzie odporność na wilgoć odgrywa kluczową rolę, na przykład w:
- materiałach filtracyjnych,
- powierzchniach samooczyszczających.
W praktyce oznacza to, że substancje takie jak oleje czy woski nie mieszają się z wodą, co czyni je niezwykle cenionymi tam, gdzie istotne są wysokie parametry odporności na czynniki zewnętrzne. W budownictwie powłoki hydrofobowe efektywnie chronią konstrukcje przed negatywnym wpływem wody, a wspomniane już powierzchnie samooczyszczające znacznie upraszczają dbanie o ich czystość. Cząsteczki z długimi łańcuchami węglowodorowymi wyjątkowo dobrze wykazują tę hydrofobową cechę. Umiejętność tworzenia i wykorzystywania materiałów hydrofobowych ma ogromny wpływ na efektywność wielu procesów technologicznych, podkreślając tym samym ich znaczenie zarówno w przemyśle, jak i w badaniach naukowych.
Jak cząsteczki chemiczne wpływają na hydrofobowość?
Cząsteczki chemiczne odgrywają kluczową rolę w kształtowaniu hydrofobowości powierzchni, co związane jest z ich momentem dipolowym oraz strukturą. W szczególności cząsteczki apolarne, pozbawione momentu dipolowego, wykazują silne właściwości hydrofobowe. Dlaczego tak się dzieje? Odpowiedź tkwi w tym, że nie potrafią one nawiązywać solidnych interakcji z cząsteczkami wody. Zwykle charakteryzują się długimi łańcuchami węglowodorowymi, które mają właściwość odpychania wody.
Z kolei cząsteczki, które zawierają grupy polarne, mają bardziej złożony wpływ na hydrofobowość. Dzięki zdolności do tworzenia wiązań wodorowych z wodą, grupy te zwiększają właściwości hydrofilowe substancji. Mimo to, jeżeli dominują niepolarnej części cząsteczki, hydrofobowe właściwości mogą pozostawać wyraźne.
Przy wyborze materiałów chemicznych, takich jak silikony czy fluoropolimery, kluczowe znaczenie ma ich wpływ na hydrofobowość powierzchni. Powierzchnie, które skutecznie odpychają wodę, znajdują szerokie zastosowanie w różnych branżach, takich jak:
- produkcja ochronnych powłok,
- technologia materiałów samooczyszczających się,
- optymalizacja procesów takich jak produkcja emulsji,
- techniki filtracyjne.
Jakie są przykłady substancji hydrofilowych?
Do substancji o właściwościach hydrofilowych zalicza się szereg minerałów, takich jak:
- gips,
- kwarc,
- kalcyt,
- dolo mit,
- anhydryt,
- magnetyt,
- hematyt,
- halit.
Te materiały potrafią skutecznie wchłaniać wodę, a ich struktura umożliwia formowanie wiązań wodorowych. Przykładem mogą być włókna celulozowe, które dzięki polarności z łatwością zatrzymują wodę. Warto również wspomnieć o nieorganicznych związkach polarowych, które cechują się doskonałą rozpuszczalnością w wodzie. Ich zdolność do współdziałania z wodą sprawia, że znajdują one szerokie zastosowanie w różnych dziedzinach, szczególnie w przemyśle chemicznym, farmaceutycznym oraz spożywczym.
Jakie są przykłady substancji hydrofobowych?
Substancje hydrofobowe to te, które mają ograniczone powinowactwo do wody. Przykłady są naprawdę interesujące:
- parafina znajduje zastosowanie zarówno w przemyśle, jak i w produkcji świec,
- siarka jest istotnym składnikiem nawozów oraz wykorzystywana w procesie produkcji kwasu siarkowego,
- rtęć obecna jest w dziedzinie medycyny i laboratoriach,
- talk zyskuje popularność dzięki swoim śliskim właściwościom w kosmetykach,
- siarczki odgrywają rolę w elektronice oraz niektórych materiałach budowlanych,
- węgiel kamienny stanowi paliwo i surowiec w chemii.
Dodatkowo, istnieje wiele cenionych minerałów, takich jak kasyteryt, ilmenit, fluoryt i szelit, które są używane w różnych gałęziach przemysłu. Diament to nie tylko piękny kamień szlachetny, ale także niezbędny w produkcji narzędzi skrawających. Z kolei złoto jest niezwykle cenione w jubilerstwie i inwestycjach. Warto również wspomnieć o włóknach syntetycznych, takich jak poliester i nylon, które znalazły szerokie zastosowanie zarówno w odzieży, jak i w przemyśle tekstylnym. Włókna szklane są istotne w budownictwie oraz przy produkcji kompozytów. Natomiast tłuszcze, w tym oleje roślinne i zwierzęce, mają właściwości niepolarne, co sprawia, że odpychają wodę.
Te hydrofobowe właściwości wynikają z ich chemicznej struktury, a niska polarność sprawia, że nie nawiązują silnych interakcji z cząsteczkami wody. Cechy te są kluczowe w różnorodnych zastosowaniach, takich jak budownictwo, medycyna czy technologia materiałowa. Dzięki hydrofobowości, materiały te sprawdzają się przy wytwarzaniu powłok ochronnych, co z kolei redukuje problemy związane z wilgocią i korozją.
Jak działają substancje hydrofilowe w wodzie?
Substancje hydrofilowe wykazują interesujące właściwości, gdy działają w obecności wody, o czym świadczy ich zdolność do zwilżania i rozpuszczania. Dzięki polarności swoich cząsteczek, skutecznie współdziałają z cząsteczkami wody, co pozwala na tworzenie stabilnych wiązań wodorowych. Przykładowo:
- białka,
- polisacharydy,
- inne substancje hydrofilowe.
Wszystkie te substancje znacząco ułatwiają transport wody w różnorodnych procesach chemicznych. Woda, jako polarne rozpuszczalnik, doskonale łączy się z tymi substancjami, co ma kluczowe znaczenie dla takich procesów jak emulsyfikacja czy transport składników odżywczych w organizmach żywych. Właściwości hydrofilowe odgrywają istotną rolę w wielu dziedzinach, w tym w farmacji, gdzie wpływają na poprawę wchłaniania leków. Ich zdolność do łatwego rozpuszczania się w wodzie wynika z uczestnictwa w reakcjach chemicznych, co z kolei wspomaga proces jonizacji. Grupy funkcyjne, które są obecne w tych substancjach, przyczyniają się do efektywnego tworzenia wiązań wodorowych. Te kluczowe interakcje mają fundamentalne znaczenie dla aktywności biologicznej oraz różnorodnych zastosowań w szerokim zakresie dziedzin. Właśnie poprzez złożone oddziaływania hydrofilowe z wodą, substancje te stają się nieodłącznym elementem nowoczesnej chemii i biotechnologii.
Dlaczego materiały hydrofilowe dobrze rozpuszczają się w wodzie?

Materiały hydrofilowe mają zdolność łatwego rozpuszczania się w wodzie, co jest efektem ich polarnej struktury. Dzięki tej właściwości mogą tworzyć stabilne wiązania wodorowe z cząsteczkami H2O. Wyrażenie „similia similibus solventur” doskonale ilustruje to zjawisko, wskazując, że substancje polarne rozpuszczają się w podobnych rozpuszczalnikach, jak woda. Wiązania wodorowe występują pomiędzy grupami funkcyjnymi tych materiałów a cząsteczkami wody, co prowadzi do silnych interakcji.
Na przykład:
- białka zawierają specyficzne grupy polarne, które znacząco zwiększają ich rozpuszczalność,
- polisacharydy również zawierają te grupy, sprzyjając ich interakcji z wodą,
- woda efektywnie przyciąga te substancje,
- ich polarność sprzyja formowaniu mikroskopijnych struktur, które stabilizują ciecz.
Oznacza to, że materiały hydrofilowe nie tylko pochłaniają wodę, ale również uczestniczą w różnorodnych procesach biologicznych i chemicznych. Wysoka rozpuszczalność tych substancji przejawia się w ich ważnej roli w reakcjach chemicznych, wchłanianiu przez organizmy oraz emulsyfikacji, co znajduje zastosowanie w przemyśle.
Dlaczego substancje hydrofobowe źle rozpuszczają się w wodzie?
Substancje hydrofobowe, różniące się od hydrofilowych, charakteryzują się niską rozpuszczalnością w wodzie z powodu swojej niepolarniej budowy. Cząsteczki tych substancji nie posiadają momentu dipolowego, co uniemożliwia im nawiązywanie wiązań wodorowych z cząsteczkami wody. Woda, będąc rozpuszczalnikiem polarnym, nie ma możliwości skutecznego łączenia się z tymi substancjami, co prowadzi do ich odpychania.
Gdy hydrofobowe cząsteczki zetkną się z wodą, cząsteczki wody są odpychane, co skutkuje powstawaniem kulistych skupisk lub kropli na ich powierzchni. Ta tendencja do formowania skupisk ogranicza kontakt z wodą, co potwierdza niską rozpuszczalność tych substancji. Do typowych przykładów hydrofobowych substancji należą:
- oleje,
- woski,
- organiczne cząsteczki z wydłużonymi łańcuchami węglowodorowymi.
Zrozumienie mechanizmów działania substancji hydrofobowych ma kluczowe znaczenie w wielu dziedzinach, takich jak chemia materiałowa, inżynieria czy procesy biologiczne w organizmach żywych. Ich właściwości są istotne nie tylko z teoretycznego punktu widzenia, ale również mają zastosowanie praktyczne, stanowiąc fundament dla licznych innowacji technologicznych.
Jak głowa i ogony cząsteczek fosfolipidów wpływają na ich właściwości?

Cząsteczki fosfolipidów posiadają niezwykłą cechę – amfifilowość. Oznacza to, że mają jednocześnie hydrofilowe głowy, które łatwo łączą się z wodą, oraz ogony hydrofobowe, które unikają kontaktu z cieczą. Ta specyfika jest kluczowa przy formowaniu błon komórkowych, ponieważ hydrofilowe części stabilizują ich strukturę poprzez przyciąganie substancji polarnych.
W wyniku tych różnic, cząsteczki układają się w podwójne warstwy lipidowe: głowy zwrócone są na zewnątrz, natomiast ogony skryte są wewnątrz. Takie ułożenie tworzy barierę, rozdzielającą wnętrze komórki od otoczenia. Interakcje między tymi dwiema częściami prowadzą do powstania błony komórkowej, która ma semi-przepuszczalny charakter.
Dzięki temu mechanizmowi możliwy jest selektywny transport substancji, co jest kluczowe dla prawidłowego działania komórek. Hydrofilowe głowy fosfolipidów umożliwiają wnikanie cząsteczek wody i innych substancji polarnych do wnętrza komórki, podczas gdy niepolarne cząsteczki są odpychane przez hydrofobowe ogony. Taka konstrukcja błon komórkowych jest istotna dla zachowania równowagi osmotycznej oraz efektywności działania komórek w różnych warunkach wodnych.
Jak cząsteczki fosfolipidów tworzą podwójną warstwę lipidową?
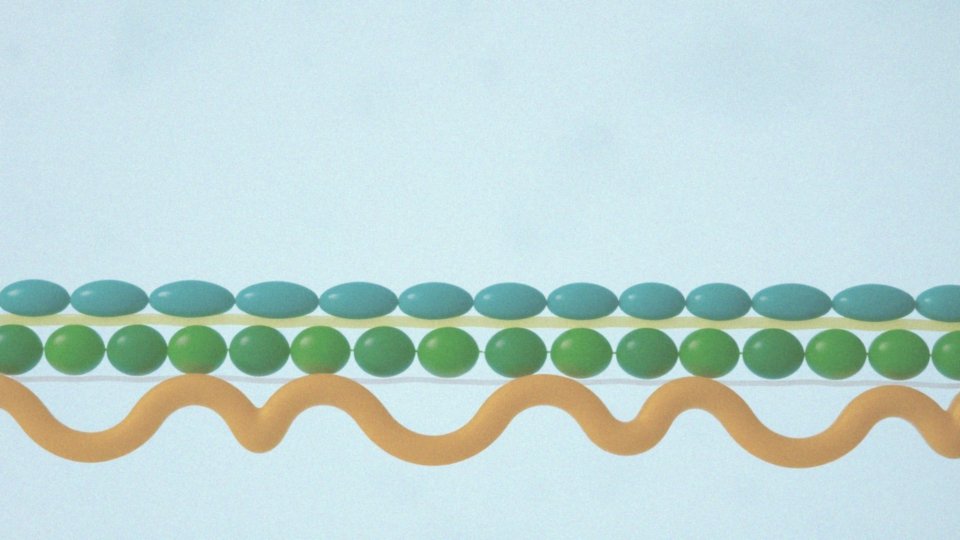
Cząsteczki fosfolipidów mają zdolność do tworzenia podwójnej warstwy lipidowej dzięki swoim wyjątkowym cechom. Składają się z:
- hydrofilowej głowy, która ma kontakt z wodą,
- hydrofobowego ogona, który od niej ucieka.
Głowy cząsteczek zajmują pozycję na zewnątrz, co umożliwia im interakcję z otaczającym środowiskiem, podczas gdy ogony znajdują się w środku, tworząc skuteczną barierę lipidową. Stabilność tej struktury wynika z polarności cząsteczek, co pozwala na utworzenie solidnej matrycy, istotnej dla funkcjonowania błon komórkowych. Tego rodzaju podwójna warstwa nie tylko oddziela wnętrze komórki od jej otoczenia, ale również reguluje wymianę różnych cząsteczek. Dlatego fosfolipidy mają kluczowe znaczenie w biologii oraz biochemii jako fundamentalny element strukturalny.
Jak różnorodność cząsteczek wpływa na zwilżalność powierzchni?
Właściwości cząsteczek mają istotny wpływ na sposób, w jaki powierzchnie wchłaniają wodę. Powierzchnie hydrofilowe, które charakteryzują się obecnością grup polarnych, łatwo wpuszczają wodę, co sprawia, że cząsteczki tego płynu formują silne wiązania wodorowe z takimi grupami. W rezultacie kąt zwilżania spada, pozwalając wodzie na równomierne pokrycie powierzchni.
Przeciwieństwem są powierzchnie hydrofobowe, w których dominują grupy niepolarne; wykazują one tendencję do tworzenia kropli, co skutkuje niskim stopniem zwilżania. Takie właściwości hydrofobowe są niezwykle użyteczne w kontekście powłok samooczyszczających, gdyż woda, spływając, skutecznie zbiera zanieczyszczenia.
Zrozumienie zjawisk dotyczących zwilżalności jest kluczowe w licznych procesach technologicznych, takich jak:
- emulsyfikacja,
- produkcja powłok ochronnych.
Właściwy wybór między materiałami hydrofilowymi a hydrofobowymi znacząco wpływa na efektywność różnych procesów produkcyjnych. Różnorodność cząsteczek nie tylko determinuję zachowanie materiałów w obliczu wody, ale także wpływa na ich funkcje i zastosowania w życiu codziennym oraz w innowacyjnych technologiach.

